給細胞做“微創手術”引發的技術革新
微創手術在如今已經是比較普及的技術了,但是如果對象是細胞呢?
近日,中國科學院深圳先進技術研究院合成生物學研究所研究員陳萬澤以共同第一作者首位,在《Nature》上發表了一篇長文,介紹了團隊在國際首創的活細胞轉錄組測序技術(Live-seq)。

偏偏是這個如此通俗易懂的名字,讓我們的認知出現了混亂。那么,團隊要克服的首要問題就是怎么在測序中維持細胞活性?利用單細胞轉錄組測序技術來觀測細胞狀態的前提,是需要將細胞裂解,提取其中的RNA來測定每個基因表達量的高低,但這樣就不能避免地殺死了細胞。經過7年的努力,陳萬澤所在課題組與瑞士洛桑聯邦理工學院Bart Deplancke課題組、蘇黎世聯邦理工學院Julia Vorholt課題組組成的團隊成功突破了這道砍。
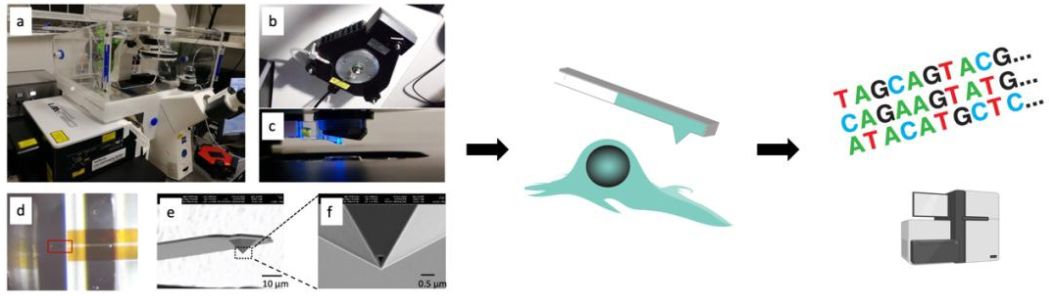
這種組合設備需要對微觀操作和極微量檢測提供解決方案:
1)具備納米級移動分辨率和皮牛頓力學靈敏度的原子力顯微鏡,實現超精密顯微操作;
2)亞皮升級別的微/納流控通道和液壓調節系統,實現微量(約1皮升)樣品提取和轉移;
3)納米級的、中空可定量的、可和細胞膜無縫密封的特殊探針,可以實現微創的細胞質提取;
4)相偶聯的實時跟蹤成像和細胞培養系統,可以長時間鎖定同一個細胞;
5)高靈敏度的RNA擴增測序;
6)對前述步驟的無縫整合
Live-seq的核心是通過對活細胞中的部分細胞質進行微創提取,從中提取出極其微量的胞質RNA進行擴增,這樣既可以從轉錄水平跟蹤細胞狀態,同時也會保持細胞的活性和功能。
當然,如此精細的操作肯定需要更加精密、分辨率更高的儀器來進行。陳萬澤剛開始嘗試利用在細胞領域相對比較小眾的原子力顯微鏡來逐漸優化自己的想法。原子力顯微鏡有一個很尖的硅探針,用于探測物質表面性質。陳萬澤團隊對這個探針進行了一系列的改造,包括表面活化、修飾等等,讓探針能夠在扎入細胞質的同時吸附出胞質內的RNA。但是改造的成本和探針成本都比較高,且成功率在當時還比較低。
之后在了解到瑞士洛桑聯邦理工學院研發了一種可以吸出部分胞質的特殊的原子力顯微鏡(FluidFM,原子力顯微鏡與微控流技術的結合),兩個團隊順理成章的開始聯合攻關。最終完成Live-seq的改造,對五種類型共295個細胞進行了測序,發現Live-seq能夠有效區分不同類型的細胞,且平均每個細胞能檢測到約4112個基因的表達信息。文章中所用的細胞包括IBA(神經膠質細胞)、ASPCs(原代小鼠脂肪干細胞和祖細胞)、RAW264.7(單核細胞或巨噬細胞樣細胞系)、RAW-G9(紅色熒光標記的Tnf啟動子,便于下游功能分析)。
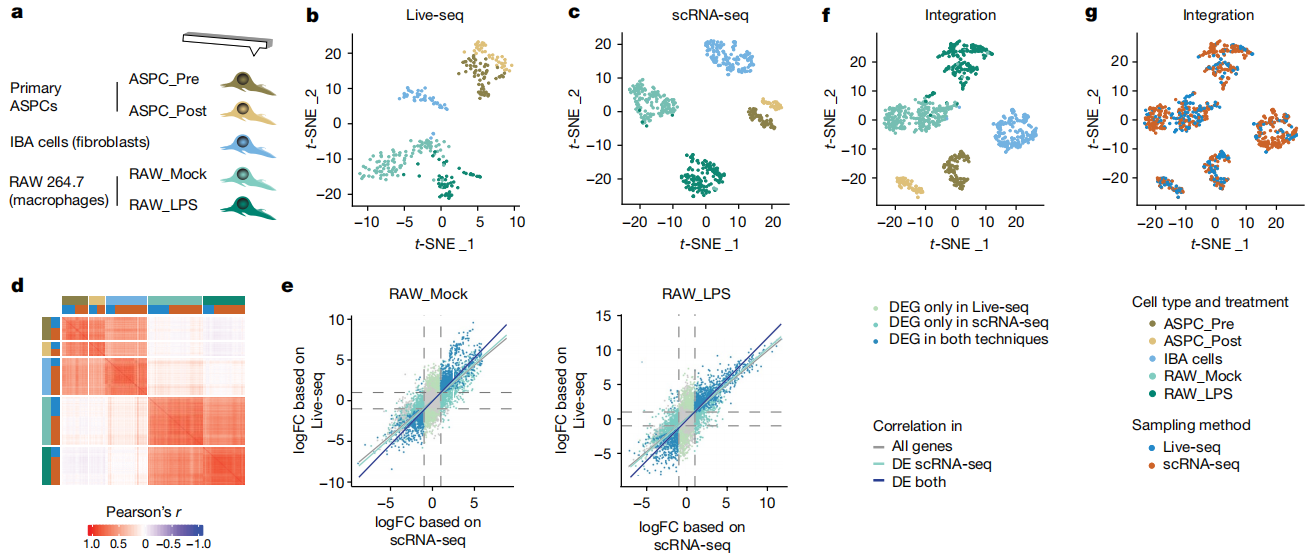
認識是實踐的目的和歸宿,一切認知都是為了讓存在的物質得以更好的存在而服務,一切認知的興盛、消亡和變遷都是為了讓存在的物質得以更好的存在而服務。Live-seq可以回答怎樣的過去決定了現在。現在Live-seq面臨的挑戰還有很多,比如高通量測序、多次同樣本采樣對細胞狀態的影響、活體體內應用,但不口否認,Live-seq的出現讓我們看到了活細胞即時狀態的數據化表征,并且為連續觀測提供了可行性方案,以及交叉學科碰撞產生的“極光”。期待Live-seq的逐漸進化、演變,甚至對細胞命運的推演。


