適者生存的理論源頭 ——細(xì)胞自噬
細(xì)胞的自噬現(xiàn)象發(fā)現(xiàn)與上世紀(jì)60年代,經(jīng)過幾十年的發(fā)展,于90年代被日本科學(xué)家大隅良典(Yoshinori Ohsumi)捧紅,并依靠對(duì)酵母細(xì)胞自噬機(jī)制的研究獲得了2016年諾貝爾生理學(xué)或醫(yī)學(xué)獎(jiǎng)。
那么什么是細(xì)胞自噬?簡單來講,細(xì)胞自噬就是細(xì)胞的自我消化,將一些暫時(shí)用不上的組分降解回收,再經(jīng)過重新組裝成自己需要的東西,廢物利用、更新?lián)Q代。細(xì)胞通過這種自我調(diào)整機(jī)制來保持細(xì)胞活力。同時(shí)也是一種應(yīng)對(duì)饑餓、機(jī)體感染等外界因素影響的應(yīng)急機(jī)制,來維持機(jī)體穩(wěn)態(tài)。
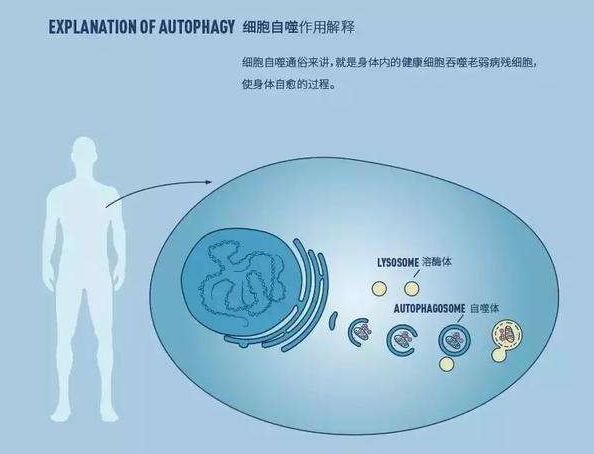 自噬分類:
自噬分類:自噬是細(xì)胞內(nèi)分解代謝的一種途徑,除此之外還有另一種我們熟知的途徑——泛素蛋白酶體途徑。細(xì)胞自噬其實(shí)分為三種方式,這是根據(jù)如何“打包”物質(zhì)和如何運(yùn)送物質(zhì)來劃分的。
第一種叫巨自噬(macroautophagy),顧名思義就是自噬體比較大,用細(xì)胞膜或者其他的雙層膜去把那些不想要的東西包裹起來,然后和溶酶體融合。
第二種叫微自噬(microautophagy),顧名思義就是自噬體比較小,溶酶體或者液泡直接用自身去吞噬那些需要降解的東西,也許是細(xì)胞器,也許是蛋白質(zhì)。
第三種叫分子伴侶介導(dǎo)自噬(chaperone-mediated autophagy),是指分子伴侶將細(xì)胞內(nèi)的蛋白質(zhì)先從折疊狀態(tài)恢復(fù)為未折疊的狀態(tài),再放到溶酶體里。
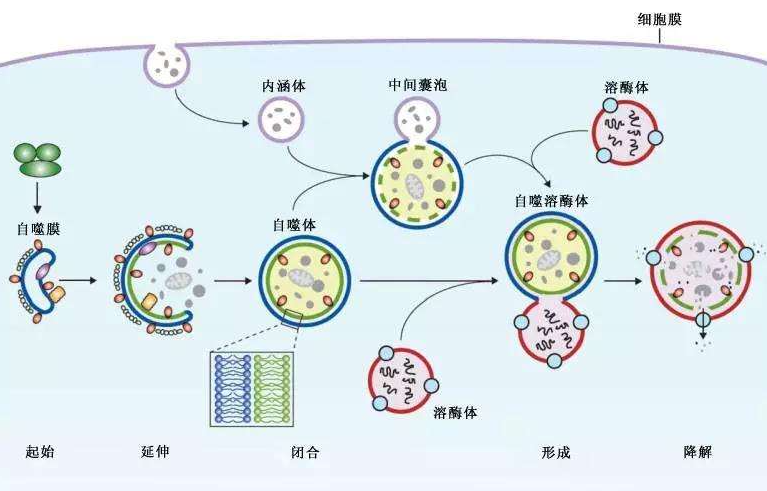 自噬的關(guān)鍵過程:
自噬的關(guān)鍵過程:自噬5大關(guān)鍵過程:(1)自噬泡(phagophore)的形成:(2)Atg5-Atg12-Atg16L復(fù)合物形成并與自噬泡融合;(3)微管相關(guān)蛋白輕鏈3(microtubule-associatedprotein light chain3,LC3)由可溶解形式(LC3-I)轉(zhuǎn)變?yōu)橹苄问剑↙C3-II),與自噬泡結(jié)合形成自噬體。(4)自噬體捕獲需降解或清除的蛋白質(zhì)、細(xì)胞器等物質(zhì);(5)自噬體與溶酶體結(jié)合形成自噬溶酶體。具體分子機(jī)制請(qǐng)看下圖。
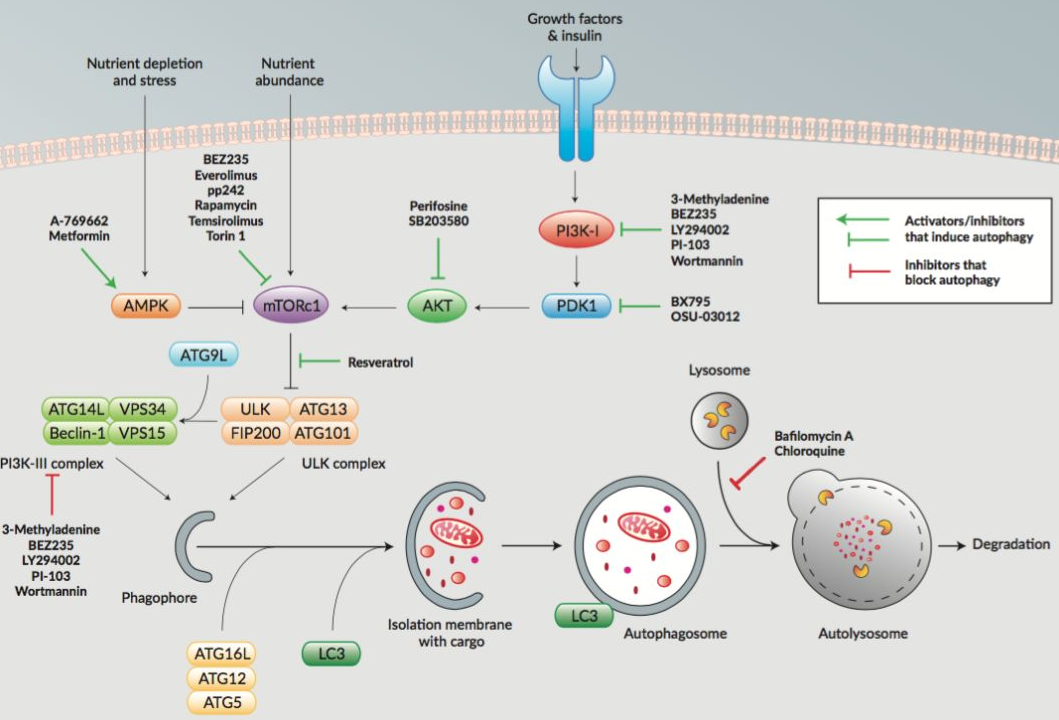
細(xì)胞發(fā)生自噬是一個(gè)非常“保守”的過程,幾乎沒有進(jìn)化。細(xì)胞自噬的出現(xiàn)是為了適應(yīng)環(huán)境,尤其是碰上了“不好的年景”,比如細(xì)胞內(nèi)細(xì)胞器損傷、異常蛋白過度積累、病原體感染、缺乏營養(yǎng)、饑餓難耐,或者細(xì)胞中氧氣、水分特別少的時(shí)候,就需要自噬了。
自噬的研究對(duì)于臨床醫(yī)學(xué)領(lǐng)域非常重要:比如,自噬功能對(duì)于癌癥具有兩面性。多種自噬機(jī)制可用于抑制腫瘤,當(dāng)細(xì)胞接受危險(xiǎn)信號(hào)時(shí),自噬機(jī)制會(huì)被啟動(dòng),去除胞內(nèi)異常的蛋白和細(xì)胞器,保護(hù)細(xì)胞免于癌變。隨著研究的深入,人們發(fā)現(xiàn)自噬水平在許多實(shí)體腫瘤中升高,特別是營養(yǎng)物質(zhì)受限導(dǎo)致癌細(xì)胞進(jìn)入休眠狀態(tài)時(shí),自噬成為癌細(xì)胞賴以生存的法寶。
再比如一些神經(jīng)退行性疾病,如阿茲海默癥(AD)最為顯著的病理特征是細(xì)胞內(nèi)MAPT/tau聚集變體及β-淀粉樣蛋白異常聚集形成β淀粉樣斑塊沉集,逐漸導(dǎo)致神經(jīng)元細(xì)胞死亡和認(rèn)知功能下降;帕金森病的病例特征是黑質(zhì)細(xì)胞區(qū)多巴胺能神經(jīng)元變性缺失和蛋白樣路易小體的形成。而神經(jīng)細(xì)胞自噬是清除胞內(nèi)異常蛋白聚集的重要途徑,提升細(xì)胞自噬能力對(duì)于神經(jīng)退行性疾病的治療意義重大。


